随机对照试验(RCT)的几点不足
随机对照试验,还是循证医学中证据等级非常高的一类研究设计类型。他的证据等级高于病例-对照研究、队列研究和非随机对照试验。小编写这个是想提醒大家,不能总把RCT供在神坛上。在仰望随机对照试验科学性的同时,别忘记这个研究类型也有这样那样的缺陷,需要正确看待和解读RCT研究的结果。
1、研究对象代表性
RCT研究虽然已经成为评估临床干预措施效果的标杆,但RCT让人诟病的一点就是研究对象代表性的问题。由于RCT往往是比较新的临床干预措施和常规措施效果有效性和安全性的差别,而且这些比较新的临床干预措施往往指的是新药。对于没有上市仍处于实验阶段的新药,其有效性和安全性都只是基于临床前研究、临床1期的试验证据;也就是就是体外实验、动物实验、健康志愿者用过这个药,在临床上开展Ⅱ期或以上的试验时,应该在病情不太重、没什么合并症、年龄不太大或太小的患者群体中开展。那么在这些RCT研究中经过“精(tiao)挑(san)细(jian)选(si)”的研究对象,往往和临床上我们面对的患者不完全一致。也就是说,RCT研究中的研究对象,不一定能代表要应用RCT研究结论的患者群。换句大白话就是,我们想寻找一款能让苹果变得更甜的化肥,但是在测试化肥效果的随机对照试验中,我们只选择了阿克苏冰糖心苹果来做试验,那红富士、嘎拉、黄香蕉、蛇果等苹果名品情何以堪呐~
2、研究设计过于严格
所谓成也萧何、败也萧何。RCT研究就是以研究设计严谨通过随机化、盲法、严格质控等措施来规范研究过程,使试验组和对照组除了研究的干预因素一项不同以外,其它特征都比较一致,提高了试验组和对照组的可比性,从而获得可靠的研究结果。但大家想过没有,由于RCT过于严格的设计往往会使研究中患者的治疗过程离真实的临床实践越来越远。比如,临床中患者往往会服用不止一种药物,但是在RCT中,往往对合并用药存在各种限制。参加过新药试验的临床大夫都知道,为了获得研究药物的“纯粹”效应,往往在研究方案、研究者手册中就明令禁止某些药物的使用。而临床上,这些病例往往是会配合这些药物使用的。那么在RCT研究中获得的有效性和安全性结果在真正的临床诊疗中往往难以重复。
3、研究终点的选择
在谈RCT试验研究终点选择之前,咱们先来普及一下两个概念:临床结局(clinical outcome)和替代终点(surrogate endpoint)。临床结局就是我们常常说的“硬终点”也就是有明确临床意义的重大临床事件,比如死亡或发病。例如高血压的临床结局应该是心血管疾病的发病率或死亡率。而替代终点往往是一些生物标志物(biomarker),它和临床结局高度相关,这个替代终点的变化往往能预示着临床结局。例如在评价AIDS的治疗效果时,我们往往选择的替代终点是CD4+T淋巴细胞数。
大家都知道,RCT研究由于设计严格、对质量控制要求很高,因此,需要花费大量的人力、物力、财力。花一、两年,甚至三、四年时间折腾就够花钱的了,如果要RCT研究中研究者都随访到患者出现临床结局,那么这其中的花费就海了去了。说白了,即使基金有这个钱支持这样的研究,那研究期限也不够随访用的。所以,通常RCT研究会选择替代终点来作为研究的主要终点(primary endpoint)。
那么作为资深粉丝,你一定能想到替代终点并不一定能代表临床结局这个point吧。一个优秀的替代终点必须①与临床结局有高度相关性,②能客观反映出干预措施对临床结局的真实、全部效应。只能遗憾的说这样的替代终点对于大多数疾病来说,仍停留在理论阶段。能完全“替代”临床结局的终点,太难找了,而RCT研究往往受条件限制难以选择临床结局来作为研究终点。那么RCT研究中干预措施的效果是否是药物真实效用的体现,仍需要仔细推敲。
简而言之,如果说RCT研究是阳春白雪,那么和咱们脚踏实地的临床实践和RCT如何对接,怎么看待RCT的结果,怎么应用RCT的结论,还是要慎之又慎。后啰嗦一句,其实RCT研究大的缺点是没经费、没人力、没临床平台的配合根本做不到,这件事我会告诉你么?
-
论文打印要求是什么,单面还是双面? 132339
-
ieee论文什么水平,含金量如何? 71501
-
医学检验期刊有哪些?论文发表难吗? 2019.11.15 17:25
-
医药卫生省级期刊发表的要求以及投稿渠道 2019.11.15 16:32
-
预防医学核心期刊发表的经验 2019.11.15 15:26
-
中国内镜杂志期刊发表的投稿要求 2019.11.15 14:32
-
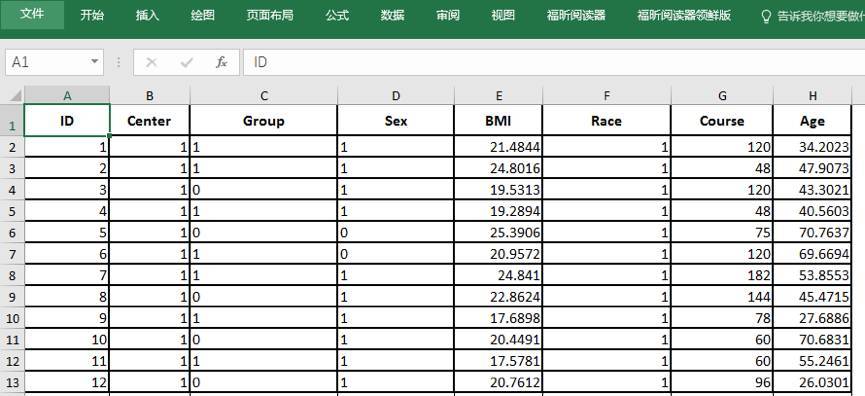 随机对照试验中缺失数据的填补
随机对照试验中缺失数据的填补 -
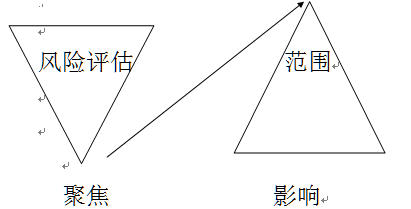 临床科研思维模式的建立过程
临床科研思维模式的建立过程